《保健食品注册与备案管理办法》自2016年7月1日正式施行[1]。保健食品是指适用于特定人群食用,具有调节机体功能,不以治疗疾病为目的,对人体不产生任何急性、亚急性或者慢性危害的食品。与普通食品相比,保健食品通常含有一定量功效成分(生理活性物质),具有调节人体特定机能的特殊功能,在当今社会逐步被广大群众所接受。碳水化合物(糖)是人类膳食的基本营养成分,具有一定的生理功能,能够增强营养和改善口感,提升保健食品的功效,是保健食品常用的添加剂。但过量的糖摄入也会带来副作用,导致高血脂、高血压等疾病,糖尿病、心血管患者不宜过量食用。因此,需要控制保健食品中各种糖的安全用量,建立准确、可靠的多种糖类的同时测定方法十分必要。
目前食品中糖类的检测方法有滴定法[2]、比色法[3]、毛细管电泳法[4]和色谱法等[5]。滴定法和比色法只能检测总糖或还原糖的含量,无法给出每种糖的具体含量。毛细管电泳的检测灵敏高,缺点是重现性差。色谱法包括离子色谱法、气相色谱法和液相色谱法,其中离子色谱检测法[6]检测灵敏度高,但糖类会在电极表面产生氧化或还原作用,影响方法的准确性。气相色谱法[7]需要将糖衍生化处理,操作较为复杂。高效液相色谱仪广泛应用于多组分复杂混合物的分离分析,糖类物质无强的紫外或可见光吸收基团,液相色谱可采用紫外衍生[8]或者荧光衍生[9]方法测定糖的含量,缺点是衍生操作的步骤复杂,影响测定结果的重现性。示差检测器是基于连续测定色谱柱流出物光折射率的变化来测定溶质浓度,具有通用性强和操作便利的优点,是推荐的国家标准方法。国家卫生部[10]和国家卫生和计划生育委员会[11]先后颁布的食品安全国家标准均采用了示差折光高效液相色谱法。示差折光检测器是通用型检测器,被测组分无需带有发色团或荧光基团,但是示差折光检测器受温度变化、溶剂极性和流动相梯度的影响较大,严重的基线漂移会降低检测结果的重现性[12]。与示差折光检测器相比,蒸发光检测器能够对所有挥发性低于流动相的物质做出准确检测,最小检测浓度可达到10-9g/ml,灵敏度高于低波长紫外和示差折光检测器,适用于糖苷、聚合物等其它检测器难以响应的化合物[13,14,15]。本研究采用液相色谱蒸发光检测器检测保健食品中常见的木糖、果糖、山梨糖、葡萄糖、蔗糖、麦芽糖、乳糖和棉籽糖,该方法具有操作简单、抗干扰能力强和准确灵敏等优点,克服现有检测方法存在的操作过程复杂,实验结果重现性差,费工耗时的缺点。
1 实验部分
1.1 仪器与试剂
高效液相色谱仪(Alliance 2695,Water公司,配Water 2424蒸发光散射检测器),在使用前经过计量公司校准,各项性能指标符合要求。色谱柱(NH2P-50-4E,Shodex公司),氮气发生器(Solaris XE,Peak公司);电子天平(BL60S,Sartorius公司);纯水/超纯水一体化系统(Direct-Q3,Merck Millipore公司);高速离心机(Sorvall LYNX6000,Thermo Scientific公司);超声-微波协同萃取仪(CW-2000,上海新拓仪器公司)。木糖、果糖、山梨糖、葡萄糖、蔗糖、麦芽糖、乳糖和棉籽糖(分析纯,Sigma公司),乙腈(色谱纯,Merck公司),无水乙醇(优级纯,北京化工厂)。
1.2 标准溶液的配制
分别精密称取8种糖标准品,超纯水为溶剂配制标准储备液(500 mg/L),4 ℃冰箱保存。临用前用流动相配制单标或者混合标准使用液。
1.3 仪器条件与参数
NH2P-50-4E色谱柱(4.6 mm×250 mm,5 μm);流动相A(0.1%三乙胺的水溶液),流动相B(乙腈),梯度洗脱程序为:0~5.0 min(15% A→20%A);5.0~15.0 min(20%A→40%A);15.0~20.0 min(40%A→15%A)。设定色谱柱温度为40 ℃,氮气压力为40 psi,加热器级别75%,漂移管温度为82 ℃,蒸发光散射检测器的增益值为100,色谱仪自动进样器的进样体积10 μl;色谱柱流速为1.0 ml/min。
1.4 样品前处理
本研究所用样品由保健食品厂家提供,样品研磨后混合均匀,精密称取2 g样品(具体称样重量视样品中糖组分的含量而定),置于锥形瓶中,加10 ml超纯水和5 ml乙醇,放置于超声辅助加热溶剂萃取仪在45 ℃条件下提取20 min,5 000 rpm/min离心,取上清液。样品重复提取三次,合并上清液并定容到50.0 ml,经0.45 μm聚四氟乙烯滤膜净化,滤液用于HPLC测定。
2 结果与讨论
2.1 条件优化
色谱柱的选择对于提高分析方法的灵敏度、选择性及分析结果的准确度具有重要的意义。与实验室常用的液相色谱烷基柱和氨基柱相比,本研究采用的NH2P-50 4E属于柱寿命更长的糖专用分析柱,兼具硅胶柱的耐压性与聚合物柱的酸碱耐受性,在梯度洗脱条件下的基线漂移更小,对多组分糖的分离度和检测灵敏度更高。蒸发光散射检测器的基线受溶剂组分和温度的影响不大,适用于梯度洗脱程序;梯度洗脱可以缩短分析周期,提高分析速度,优化后的梯度洗脱程序如1.3所示。
漂移管温度和氮气流速是影响蒸发光散射检测器的最重要因素,在实验过程中需要精确控制氮气压力和漂移管温度,尽量形成较大尺寸的颗粒和较窄的粒度分布,从而获得较高的检测灵敏度。以检测结果为指标,单因素实验发现氮气的压力为40 psi,加热器级别75%,漂移管温度为82 ℃时蒸发光检测器响应信号具有较高的信噪比,检测结果的精密度和准确度更好。
2.2 标准曲线的建立
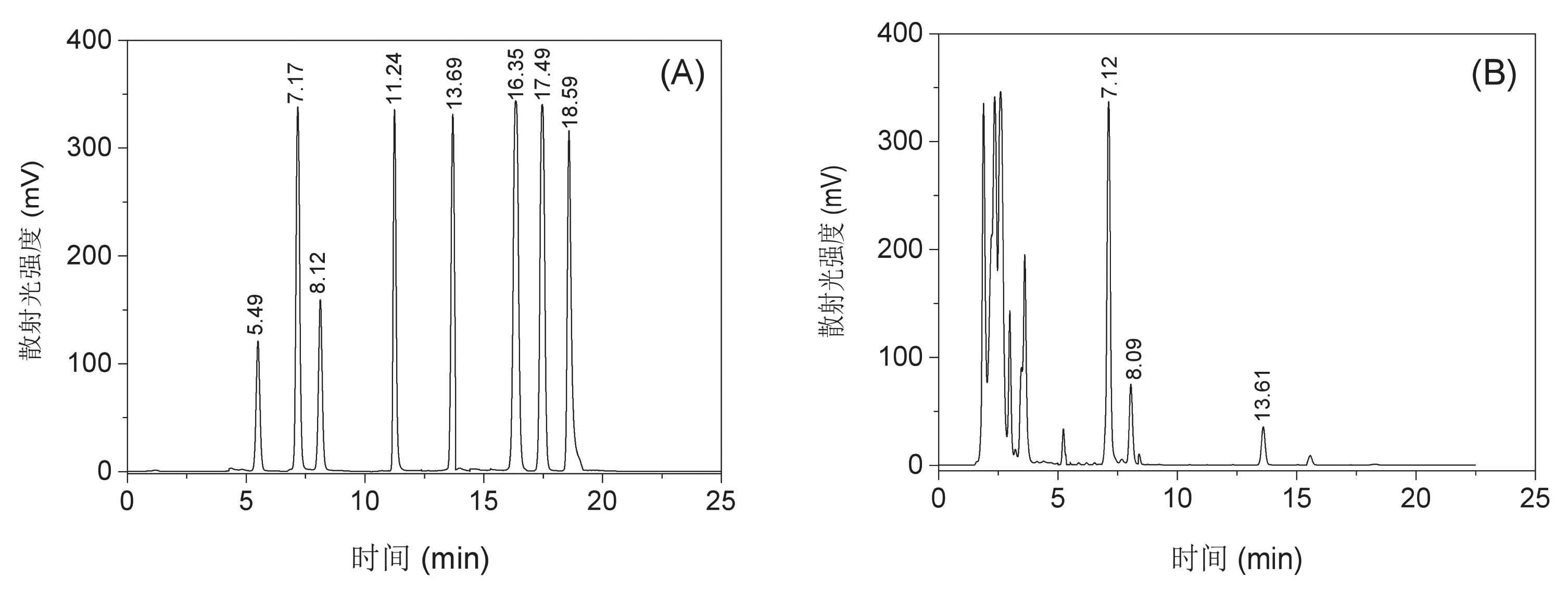
按照1.3部分设定的仪器条件,对8种糖标准溶液单独进样,依据色谱图的保留时间对每种糖做定性分析。配制8种糖的混合标准溶液,混合标准溶液进样后的色谱流出曲线如图1A所示,木糖、果糖、山梨糖、葡萄糖、蔗糖、麦芽糖、乳糖和棉籽糖的保留时间分别为5.49、7.17、8.12、11.24、13.69、16.35、17.49和18.59 min。8种糖组分在该色谱体系的分离度>1.5,实现了基线分离,满足多组分物质定量分析的基本要求。同时将建立的分析方法应用于保健食品的测定,样品色谱图见图1B所示,在22 min内,保健食品中含有的果糖、山梨糖和蔗糖组分与杂质得到了基线分离,色谱峰呈良好的正态分布,加标样品中8种糖的出峰时间与单标准溶液的保留时间基本一致(相对偏差<1.0%)。
图1 8种糖的蒸发光散射液相色谱图
注:其中A图是8种糖混合标准色谱图,B图是样品色谱图
蒸发光散射检测器的工作原理是加热蒸发流动相溶剂,样品在蒸发室内形成溶质颗粒而产生光散射效应,测定散射光强度获得组分的浓度信号。散射光的强度与组分质量浓度的指数次方呈正比关系,见表1。以标准品峰面积的常用对数为纵坐标,以标准品溶液的浓度(μg/ml)的常用对数为横坐标作图,以最小二乘法进行线性回归,得到8种糖的线性方程。可以看出,在5.0~400.0 mg/L质量浓度范围内,蒸发光散射检测器响应值的常用对数分别与保健食品中8种糖质量浓度的常用对数呈线性关系,拟合时要求线性相关系数达到0.995以上,其中的X和Y分别代表测定组分质量浓度的常用对数和色谱峰面积的常用对数。木糖、果糖、山梨糖、葡萄糖、蔗糖、麦芽糖、乳糖和棉籽糖的最低检测质量浓度范围为5.0~20 mg/L,以3倍噪声水平相当的响应峰高值所对应的待测物质浓度作为检出限,由结果可见,该方法有较宽的线性范围和重现性。
表1 8种糖的液相色谱-蒸发光散射检测标准曲线的线性范围、回归方程、检出限和精密度 导出到EXCEL
成分 |
线性范围(mg/L) |
回归方程(Ln~Ln) |
检出限(mg/L) |
精密度(%) |
|
木糖 |
20.0~400.0 |
Y=1.15X+4.96 |
5.0 |
1.3 |
果糖 |
10.0~00.0 |
Y=1.22X+4.73 |
3.0 |
1.1 |
山梨糖 |
10.0~200.0 |
Y=1.27X+4.68 |
3.0 |
0.9 |
葡萄糖 |
10.0~200.0 |
Y=1.26X+4.83 |
3.0 |
0.8 |
蔗糖 |
5.0~100.0 |
Y=1.43X+4.36 |
2.0 |
0.7 |
麦芽糖 |
10.0~200.0 |
Y=1.31X+4.87 |
3.0 |
0.9 |
乳糖 |
10.0~200.0 |
Y=1.29X+4.65 |
3.0 |
1.1 |
棉籽糖 |
20.0~400.0 |
Y=1.16X+4.93 |
5.0 |
1.2 |
分析方法的精密度可以通过对样品的多次平行测定计算标准偏差予以评估。在空白样品中加入8种对照品混合溶液(其中含8种多糖的浓度为50.0 mg/L),平行测定7次,计算精密度(RSD,相对标准偏差),结果如表1所示,8种糖的平行测定相对标准偏差均<1.5%,表明所建立的方法重现性较好,分析方法的精密度满足食品卫生分析的基本要求。
2.3 样品分析
本研究采用1.4所建立的前处理方法采用水溶剂提取保健食品中添加的糖成分。由于糖易溶于水,水溶剂可充分提取样品中存在的糖,样品中加入的乙醇可以降低保健食品中蛋白质在水中的溶解度,减少蛋白质对检测结果的干扰。升高温度和超声波辅助可加速糖的溶出,但温度过高会加快多糖、蔗糖和麦芽糖的水解,选择超声辅助加热萃取仪的温度为45 ℃。对于某些糖含量高的样品,需要用流动相将样品萃取液稀释到标准曲线线性范围后测定。
测定样品的加标回收率可评估检测方法的准确性,精密称取固体保健食品样品2.0 g,将样品前处理并定容到50 ml,对于样品中含有的糖组分,加标量与样品糖含量接近,高浓度样品需要稀释到标准曲线的浓度范围。对低于检出限的糖组分,按照检出限含量的10倍含量添加标准物质。在样品中加入8种糖,按照回归方程测定并计算加标回收率,结果见表2,糖的加标回收率的范围为86.7%~104.5%,该方法对保健食品中糖的检测具有较高的准确度。
表2 样品中8种糖的加标回收实验 导出到EXCEL
样品 |
木糖 |
果糖 |
山梨糖 |
葡萄糖 |
蔗糖 |
麦芽糖 |
乳糖 |
棉籽糖 |
原有量(mg) |
— |
48.5 |
— |
70.3 |
35.6 |
— |
— |
— |
加入量(mg) |
2.5 |
48.5 |
1.5 |
70.3 |
35.6 |
1.5 |
1.5 |
2.5 |
测得量(mg) |
2.3 |
103.5 |
1.3 |
139.7 |
72.3 |
1.4 |
1.3 |
2.4 |
回收率(%) |
92.1 |
104.5 |
86.7 |
99.4 |
101.5 |
93.3 |
86.7 |
96.0 |
注:表中—表示在方法检出限以下。
3 结 论
蒸发光检测器对温度和压力变化没有过高要求,梯度洗脱时基线稳定,响应值高、分离效果好、结果准确和重现性好等诸多优点,可以用于保健食品中多种糖的同时测定。本研究采用NH2P-50 4E糖专用色谱柱,梯度洗脱法分离保健食品中的8种糖,建立了保健食品中8种糖的多组分同时检测技术。蒸发光散射检测器的响应值峰面积的对数(Ln)与保健食品中8种糖的质量浓度的常用对数(Ln)线性相关,其中木糖、果糖、山梨糖、葡萄糖、蔗糖、乳糖、麦芽糖和棉籽糖的检出限为5.0~20 mg/L,样品测定的精密度<1.5%,加标回收率为86.7%~104.5%。本研究所建立的检测方法具有灵敏度好、准确度高、试剂用量少、仪器自动化程度高、操作简单、分析速度快等优点,适用于保健食品中多种糖的同时测定。